Perché il CBD (cannabidiolo) sembra proteggere i neuroni in alcuni casi, mentre causa la morte cellulare in altri? Una nuova ipotesi, contenuta in un documento teorico di Anthony J. Vasquez Sr. della Delaware Valley University, pubblicato su Reddit, propone una risposta unificante: il CBD agisce come un test di stress mitocondriale, i cui risultati sono determinati non solo dalla dose, ma anche dallo stato metabolico preesistente della cellula.
Il modello a due vie proposto mira a chiarire ciò che i ricercatori hanno a lungo descritto, spesso in modo vago, come “farmacologia dipendente dal contesto”.
Dalla neuroprotezione all’apoptosi
La ricerca clinica e preclinica ha ripetutamente evidenziato il profilo paradossale del CBD, talvolta descritto come bifasico per i suoi diversi effetti a seconda della dose: energico a piccole dosi, calmante a dosi elevate.
Nel caso dell’epilessia, il CBD purificato ha ridotto significativamente la frequenza delle crisi in pazienti pediatrici resistenti al trattamento (Devinsky et al., 2017). Al contrario, studi di laboratorio dimostrano che il CBD può indurre l’apoptosi nel glioblastoma e in altre linee cellulari tumorali attraverso l’interruzione mitocondriale (Massi et al., 2013).
È importante notare che questi effetti si verificano talvolta in intervalli di concentrazione sovrapposti. Come scrive l’autore, non si tratta semplicemente di una questione di dose-risposta, ma di un fenomeno di risposta contestuale.
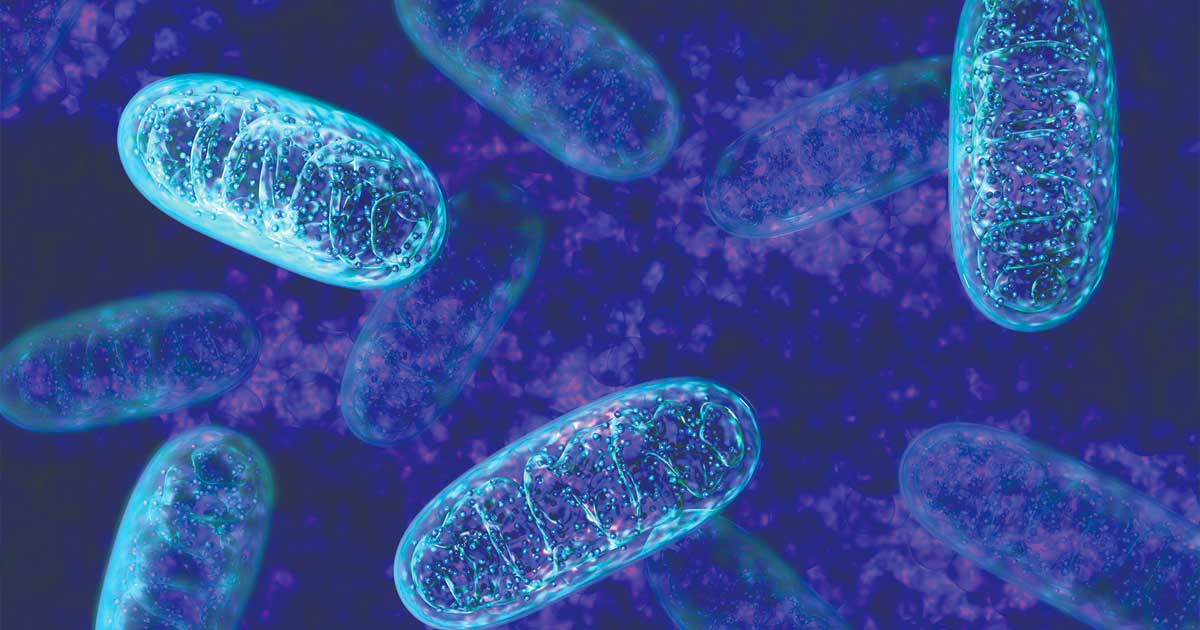
La CBD interagisce con più di 60 bersagli molecolari, tra cui TRPV1, 5-HT1A, PPARγ, GPR55, recettori dei cannabinoidi e proteine mitocondriali come VDAC1 (canale anionico voltaggio-dipendente 1). Questa promiscuità molecolare ha reso difficile chiarire i meccanismi.
Il nuovo quadro propone che la variabile chiave non sia il solo bersaglio, ma lo stato mitocondriale della cellula esposta.
Il modello a due vie

Il modello perfezionato distingue due meccanismi dipendenti dalla concentrazione:
1. Percorso terapeutico (1-5 μM)
A concentrazioni più basse, terapeuticamente rilevanti, il CBD si impegna preferenzialmente con bersagli ad alta affinità come TRPV1, 5-HT1A, PPARγ e GPR55. Queste interazioni sono associate a effetti antinfiammatori, ansiolitici e neuroprotettivi.
All’interno di questo intervallo, l’alterazione mitocondriale è limitata e le cellule con riserve bioenergetiche sane possono tamponare lo stress transitorio.
2. Via citotossica (10 μM)
A concentrazioni più elevate, il CBD raggiunge un’occupazione significativa di VDAC1, una proteina incorporata nella membrana mitocondriale esterna e spesso descritta come il “guardiano mitocondriale”.
Il legame diretto CBD-VDAC1 è stato misurato con una costante di dissociazione di circa 11 μM (Rimmerman et al., 2013). Un legame di questo livello altera il potenziale di membrana mitocondriale, altera l’omeostasi del calcio e può innescare il rilascio di citocromo c, causando infine l’apoptosi.
Le cellule già sottoposte a stress metabolico, come molte cellule tumorali con specie reattive dell’ossigeno (ROS) elevate e potenziale di membrana instabile, sembrano essere particolarmente vulnerabili. In questi sistemi, il CBD può spingere la bioenergetica oltre la soglia di sopravvivenza.
Da questo punto di vista, la CBD non “colpisce” selettivamente le cellule tumorali. Piuttosto, amplifica la fragilità metabolica sottostante.
Convalida della letteratura e convergenza computazionale
L’articolo passa in rassegna oltre 70 pubblicazioni che esaminano i meccanismi cellulari della CBD. Secondo l’autore, 18 delle 20 previsioni seguite corrispondevano ai dati pubblicati, tra cui:
- Effetti mitocondriali rapidi che si verificano entro pochi minuti dall’esposizione
- Aumento della sensibilità in cellule metabolicamente pre-stressate
- Attenuazione della citotossicità con gli inibitori di VDAC1 come DIDS o VBIT-4
- Consistenti cambiamenti nel potenziale di membrana, nella produzione di ROS e nel flusso di calcio
Oltre alla sintesi della letteratura, l’ipotesi è stata valutata utilizzando un protocollo di convergenza AI multi-modello noto come IRIS Gate Evo. Cinque modelli linguistici indipendenti di grandi dimensioni sono stati interrogati sul quesito di ricerca e, secondo quanto riferito, hanno convergono sulla stessa struttura bidirezionale, compresa l’identificazione di VDAC1 come “interruttore” dose-dipendente.
Sebbene la convergenza computazionale non sostituisca la validazione di laboratorio, rafforza la coerenza interna del quadro proposto.
Una lacuna sperimentale critica
Nonostante il forte sostegno a un ruolo del VDAC1 nella citotossicità indotta dal CBD, l’articolo identifica una notevole omissione nella letteratura: nessuno studio pubblicato ha testato se il blocco del VDAC1 elimini gli effetti neuroprotettivi del CBD a basse dosi. Questo esperimento permetterebbe di mettere direttamente in discussione o confermare il modello bidirezionale.
Se l’inibizione di VDAC1 non influisce sulla neuroprotezione, ciò confermerebbe l’idea che gli effetti protettivi siano mediati indipendentemente da TRPV1, 5-HT1A o PPARγ. Se la protezione viene meno, il modello deve essere rivisto.
Entrambi i risultati chiarirebbero il meccanismo del CBD.
Implicazioni cliniche: targeting metabolico
Se convalidato, il modello suggerisce che la selettività terapeutica potrebbe essere ottenuta non da bersagli molecolari specifici del cancro, ma dalla vulnerabilità metabolica. I tumori con mitocondri disfunzionali potrebbero essere sensibilizzati selettivamente ad alte dosi di CBD o a trattamenti combinati che aumentano lo stress ossidativo.
Il quadro evidenzia anche potenziali biomarcatori per prevedere la risposta, tra cui l’integrità del DNA mitocondriale, il fenotipo metabolico del tumore e le varianti genetiche del CYP450 che influenzano il metabolismo della CBD.
Un test di resistenza, non un proiettile d’argento

L’articolo conclude che il CBD non deve essere considerato un composto universalmente protettivo o distruttivo. Piuttosto, funziona come amplificatore bioenergetico, rivelando se una cellula è in grado di sopportare un disturbo metabolico.
Per i medici e i ricercatori, questo nuovo approccio potrebbe contribuire a spostare il dibattito oltre gli “effetti dipendenti dal contesto” verso parametri mitocondriali misurabili e meccanismi dose-specifici.
Come sottolinea l’autore, questi risultati rappresentano un’ipotesi meccanicistica e non una raccomandazione clinica. Tuttavia, collegando la dose, l’impegno di VDAC1 e lo stato mitocondriale in un quadro coerente, il modello a due vie offre una spiegazione verificabile per uno dei paradossi più persistenti nella scienza dei cannabinoidi.

 Business4 settimane ago
Business4 settimane ago
 Cannabis in Francia3 settimane ago
Cannabis in Francia3 settimane ago
 Cannabis in Francia3 settimane ago
Cannabis in Francia3 settimane ago
 Canapa1 settimana ago
Canapa1 settimana ago
 Cannabis nei Caraibi3 settimane ago
Cannabis nei Caraibi3 settimane ago
 Cannabis medica3 settimane ago
Cannabis medica3 settimane ago
 Cannabis3 settimane ago
Cannabis3 settimane ago
 Cannabis in Francia2 settimane ago
Cannabis in Francia2 settimane ago



















You must be logged in to post a comment Login